紫外線と赤外線について皆さんはどのようなイメージをもたれるでしょうか
日焼けを起こしそうな方を選ぶとしたら、それは紫外線であるというイメージをもたれる方が多いのではないでしょうか
これは、紫外線のもつエネルギーが大きいためです
光を波長の大小に従って並べると、エネルギーの大きい方(または波長の短い方)から、紫外線・青色光・緑色光・赤色光・赤外線という順番になります
具体的には、青色光であれば400 nm程度、赤色光であれば800 nm程度と考えると、覚えやすいでしょう(筆者は大学のころ、このようにレーザー分光学のS教授に習いました)
そして日焼けを起こすようなエネルギーの高い光は、当然、光反応を起こしやすいということになります
ですので、紫外線・青色光などといった高いエネルギーの光は、実は日焼けを起こしてしまうというリスクがあるだけでなく、有用な光反応を起こすためにも用いられます
反対に、波長が2倍程度長い赤色光などといった低エネルギー光は、エネルギーが2分の1倍になってしまいますから、紫外線のような光反応を起こすことはできません
ならば、我々は危険性の高い紫外線や青色光のみに頼って生き続けるしかないのでしょうか??
実は、そんなこともありません
これを解決する研究が、近年報告されてきています
これらの研究は、可視光のような低いエネルギーの光を、紫外線でしか起こせなかった反応に適用するという試みに成功しています
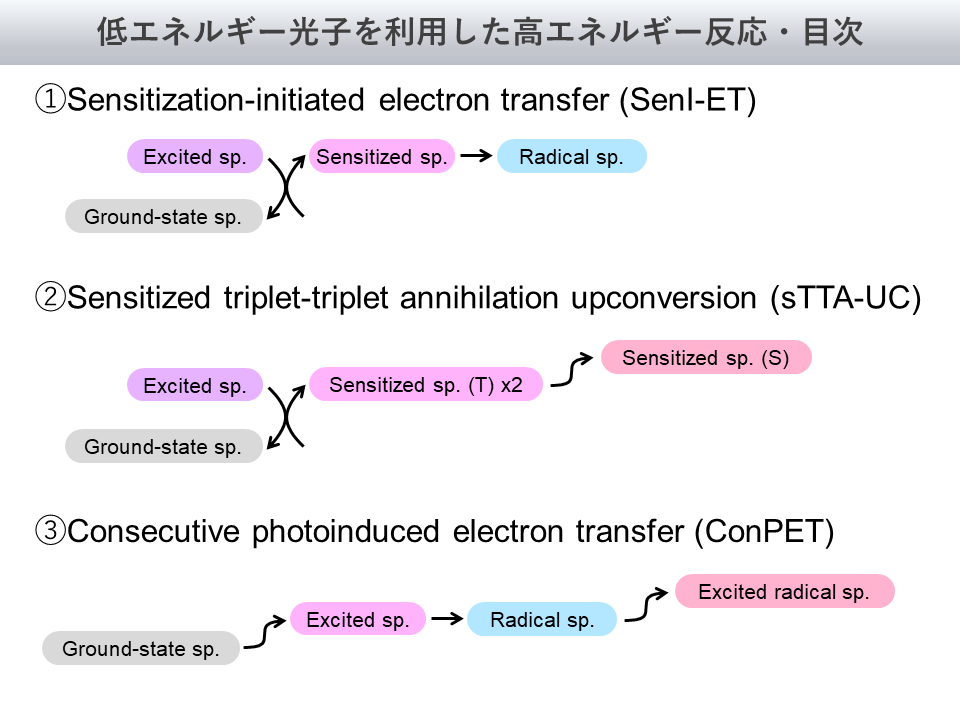
本記事では、この「低エネルギー光子を利用した高エネルギー反応」について、よく知られている以下の3つの手法を実例に沿って解説します
それぞれ、①Sensitization-initiated electron transfer (SenI-ET)、②Sensitized triplet-triplet annihilation upconversion (sTTA-UC)、③Consecutive photoinduced electron transfer (ConPET)という手法です
画像には矢印でエネルギーの流れを記載していますが、高い位置にあるものほど高いエネルギーを有しており、反応が有利になると解釈してください
以下、これらについて順に説明する前に、Photoredox触媒に関する前提知識を共有しておきます
図2左の通り、多くの場合Photoredox触媒は、その基底状態においては還元剤(reductant)や酸化剤(oxidant)に対し不活性であります
これは、反応物質同士のHOMO-LUMOギャップが大きく、電子のやりとりが起きにくいためです
しかしPhotoredox触媒が励起されると(図2右)、もとのHOMOが電子を受け入れたり、もとのLUMOが電子を与えられるようになり、反応が進行可能となります
このような原理に基づき、Photoredox触媒は光照射を起点とした化学反応を起こします
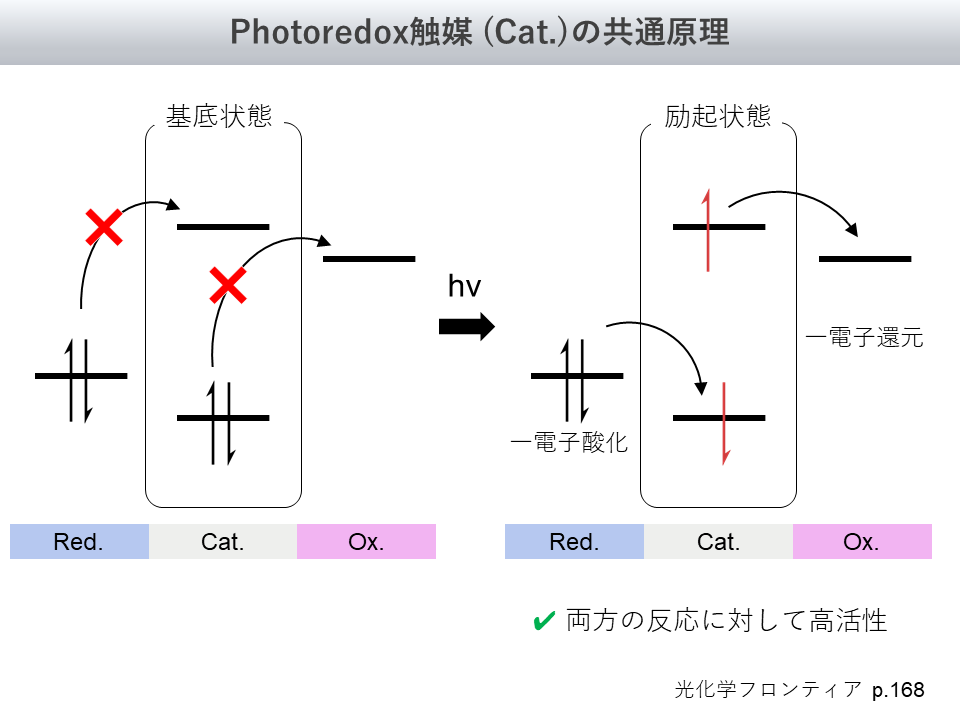
以上の前提知識を踏まえた上で、以下の①SenI-ET、②sTTA-UC、③ConPETについてご覧ください
①Sensitization-initiated electron transfer (SenI-ET)
SenI-ETは、日本語では、「光増感によって開始される電子移動」という意味になります
光増感とは、光励起した分子のエネルギーが、エネルギー移動を介して他の分子に伝わり、間接的にその他の分子が励起されることです
この例として代表的な、ルテニウム錯体とピレンの活用例について、そのメカニズムがどのように明らかにされてきたかを見ていきましょう
この初の報告例は、2017年にBurkhard KönigらによってAngew. Chem.に報告された例[1]です
この例の、従来型メカニズムとの対比を図3に示します
この研究のうまみは、Ru錯体のみでは進行させられない光反応を、ピレン(Py)と組み合わせることによって進行させることにあります
従来の場合ですと、Ru錯体の青色光励起によって得られるRuラジカルアニオンの還元電位は-1.3 Vと小さく、還元できる基質範囲に限界がありました(図3左)
かといって、還元力の高いピレンの活性種を得ようとしても、必要な光は紫外光というエネルギーの高いものになってしまいます(黄色固体なら青色光を吸収していることになりますが、白色固体であるPyが吸収できる光はせいぜい365 nmくらいまでです)
エネルギーの高いものを使えば反応を進行させやすくなるのは当たり前なことですから、これでは面白くありません
ですので、理想的には、青色光という比較的低エネルギーな光を使ってRu錯体を励起させ、その後なんとかしてPyにエネルギーを移し、還元力の高いPyの活性種に光反応を起こさせるというスキームが望ましいです
これが図3右のスキームに相当します
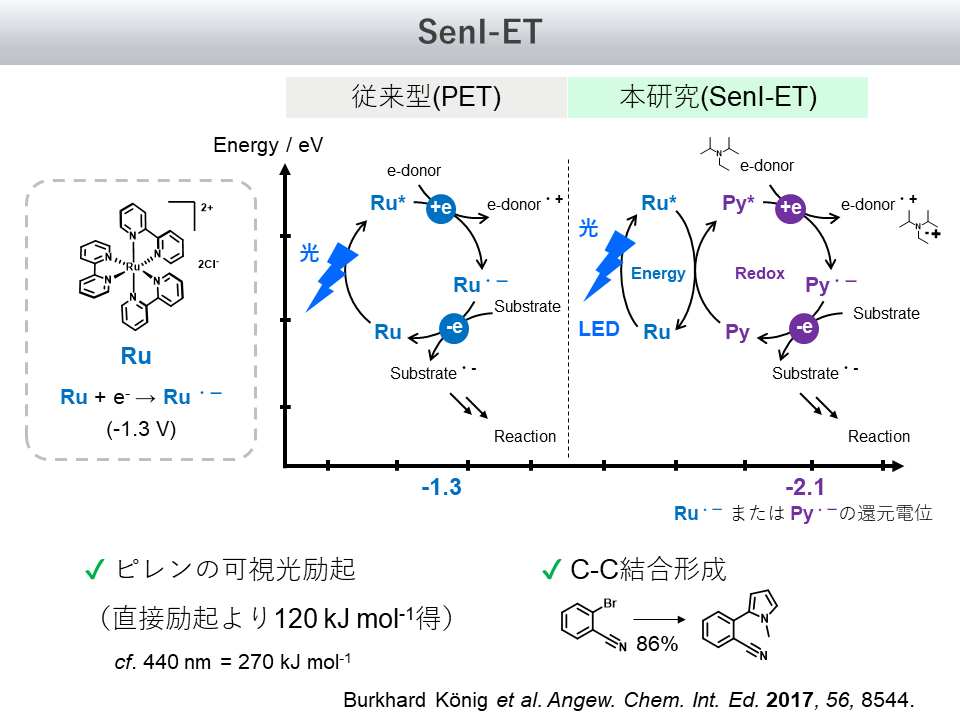
図3右側の詳細を述べます
まず、Ruは光励起によって励起状態になります
その後、励起状態のRuから基底状態のPyへエネルギー移動が起き、Pyは励起状態になります
励起状態のPyは電子を受け取りやすい性質があるため、電子ドナーであるアミンから一電子奪い、Pyのラジカルアニオンとなります
その後Pyのラジカルアニオンは基質を還元し、目的の光反応を進行させるという仕組みです
実際に、これによって高い収率でC-C結合の形成が達成されています
また、この反応では通常紫外光しか吸収しないPyを青色光で励起できたことと等価になりますが、このような間接的な励起は直接励起するよりも120 kJ/molほどお得です(O-O結合1個分くらいです)
さらっと説明してしまいましたが、このお得な反応は本当にこれほど単純なメカニズムなのでしょうか?
実のところ、このメカニズムに対して異を唱えた研究者たちが存在します
Vincenzo Balzani氏のグループになります
その根拠となる図4の内容は、1報目の例に引き続いてAngew.誌に掲載されたものです[2]
図4を見ると、Pyの励起状態(T1状態)からPyのラジカルアニオンとアミンのラジカルカチオンを生じる過程は、熱力学的に不利であることが確認できます
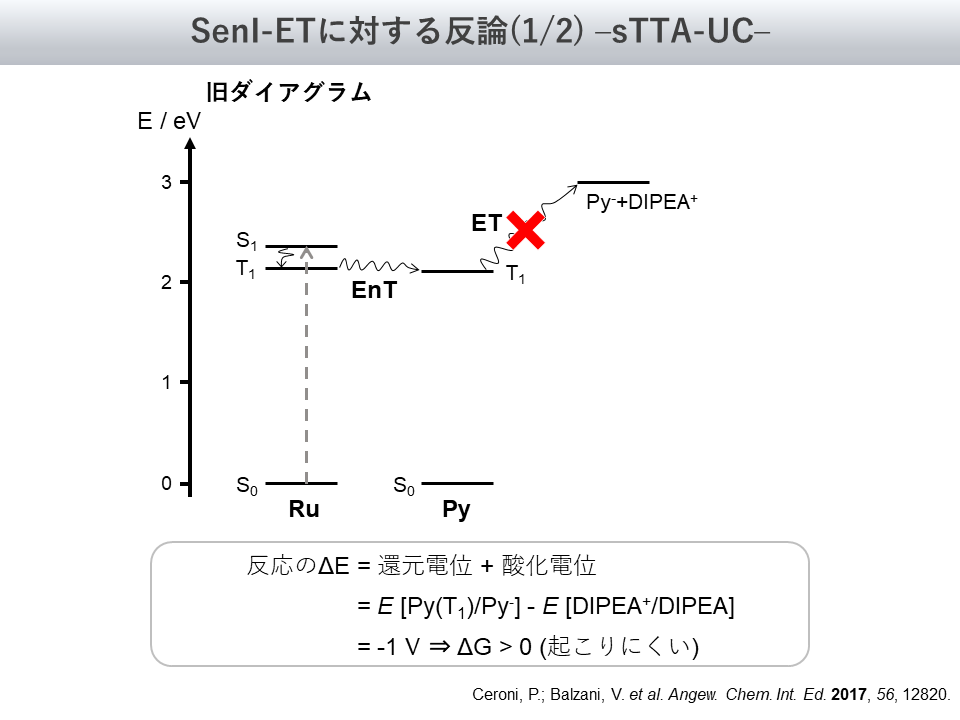
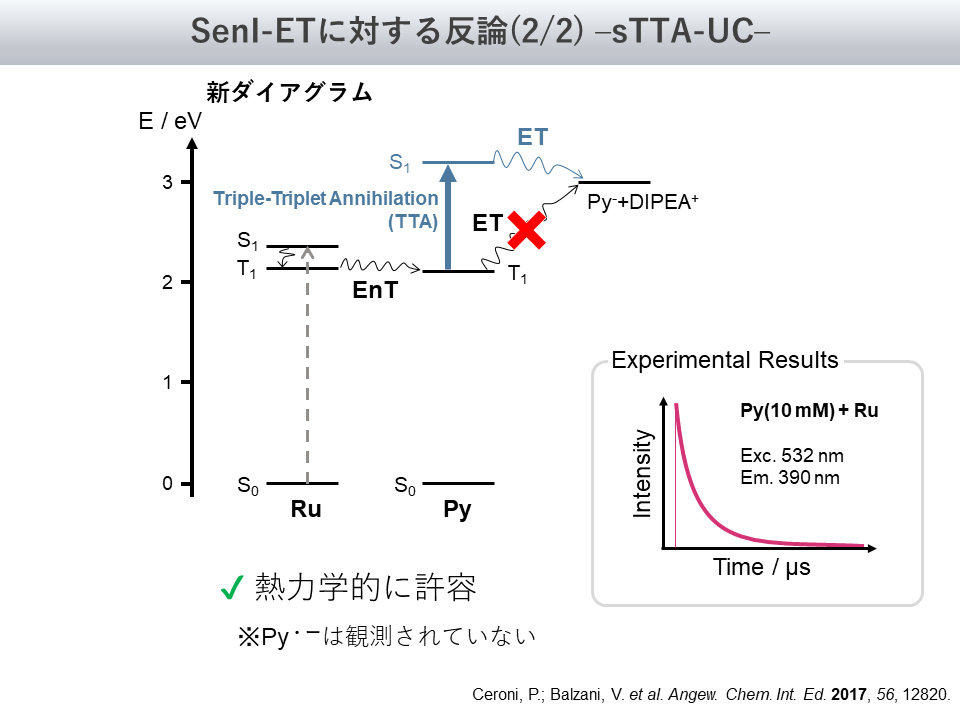
そこでこの代替案として、Ceroni氏、Balzani氏のグループから提唱されたメカニズムが以下の図5です
このメカニズムでは、二つある三重項Pyから一つの一重項Pyが生成し(triplet-triplet annihilation, TTA)、この一重項Pyから一電子がアミンに渡されます
これならば、一重項Pyのエネルギーが十分に高く、反応が熱力学的に許容になるというわけです
実験的事実としては図5右下にあるように、PyとRuの混合溶液に対し532 nm光でRuを選択的に励起すると、Pyからの発光である390 nm光が観測されています
Pyの三重項は発光できない一方、その一重項は発光できることから、この事実は一重項Pyが系中に存在していたことを示します
したがって、本反応機構の推定メカニズムが改められたということになります
ところが、以上の反論に対するさらなる反論が、König氏からAngew.誌に発表されます[3]
König氏の主張をまとめると、
- TTAはレーザーで反応を開始させないと困難である。[4]
- 一重項励起状態のPyがもし生成しているなら、この化学種はアミンがなくとも基質を還元できる。一方で、実際にはアミンが必要である。このことから、一重項励起状態のPyは今回の結果に直結しているとは言えない。
- 反応系の環境によって電位は大きく変わるため、必ずしもその議論通りにはならない。
といった具合です。
そして、最初の報告では記載していなかった新たな推定メカニズムを掲載しました。
これが図6左になります。順に説明すると、
- Ru錯体が光励起
- 励起Ru錯体からのエネルギー移動によって、三重項励起状態のPyが生成
- 加えて、励起Ru錯体はアミンから電子を受け取り、1価のRu錯体も生成
- 2と3のステップでそれぞれ生成した励起状態のPyと1価のRu錯体が反応し、Pyのラジカルアニオンを生じる(この反応は1.23 Vというかなり発熱的な反応であり、有利に進行する)
- Pyのラジカルアニオンによって基質が還元され、生成物に至る
というメカニズムになります。大分、複雑になりました。
これで、本反応の進行の仕方には①sTTA-UC機構と②SenI ET機構の2通りがあり得ることとなったわけですが、それぞれがどれくらい進行しているかを実験的に検証した研究者がいます
それは、Evan Moore氏のグループです
彼らによって、ありえる2つのパスがどれくらいの速度で進行しているかが、ナノ秒過渡吸収分光法(ns-TA)を用いて定量されました[5]
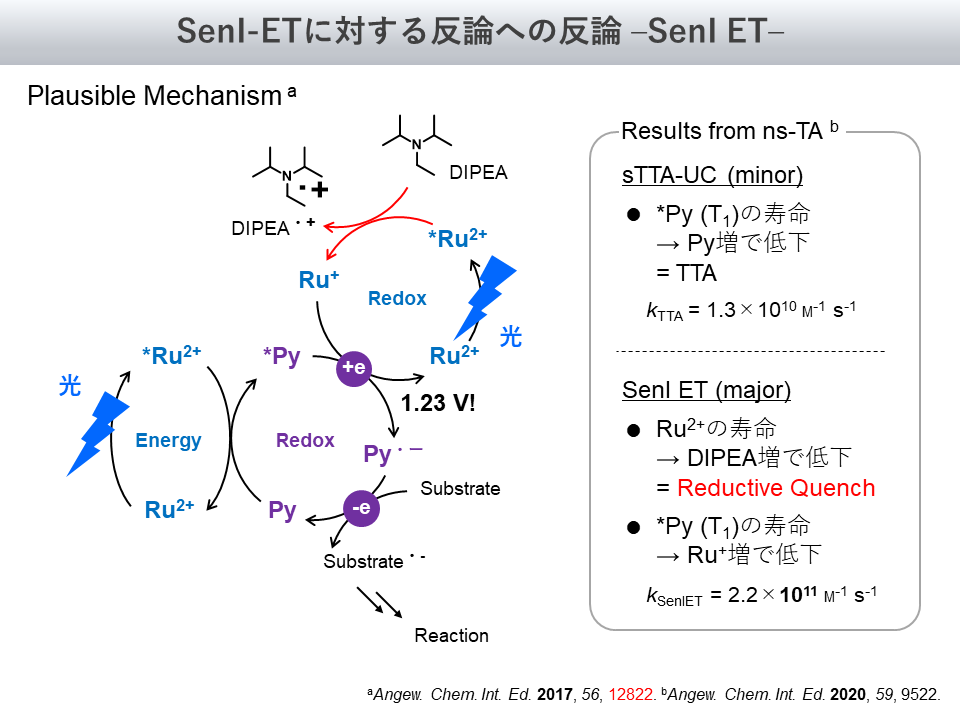
具体的には、sTTA-UCの速さについては、Py濃度に対する*Py(T1)の寿命を測定することで考察できます
また、SenI ETの速さについてはアミン濃度に対するRu2+の寿命や、Ru+濃度に対する*Py(T1)の寿命を測定することで考察できます
測定の結果、kTTAとkSenIETは、それぞれ1.3×1010 と 2.2×1011 M-1 s-1であり、SenI ETの速さの方がTTAの速さを上回ることが示されました
したがって、2つ提唱されたメカニズムのうち、めでたくSenI ETの方が主要(major)なパスであることが明らかになったというわけです
②Sensitized triplet-triplet annihilation upconversion (sTTA-UC)
二つのtriplet化学種から一つのsinglet化学種を生じ、光子のエネルギーをより高い状態へと変換する機構をsTTA-UCと言います
前の項目ではSenI ET機構を主軸とした可視光による分子変換が達成されたことを述べましたが、sTTA-UC機構をmajorなパスとする反応も存在し得るのでしょうか?
実は、反応系をうまくデザインすることで、sTTA-UC機構も有効なエネルギー変換法となることが、2021年にOliver Wenger氏のグループから報告されました[5]
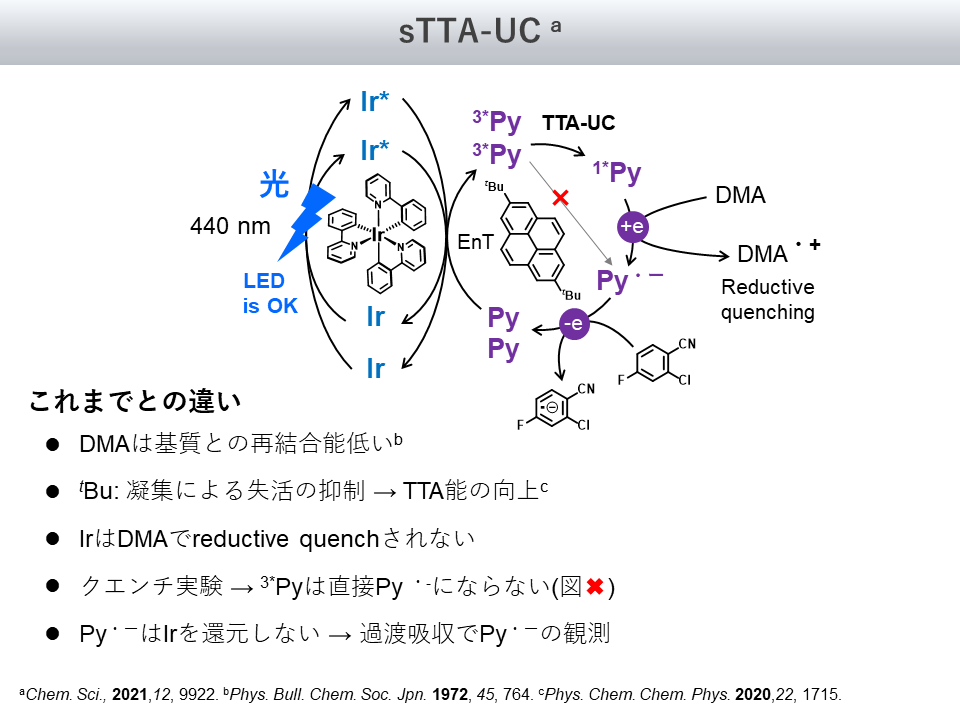
反応機構は図7に示す通りで、錯体・ピレン・アミンの全ての分子設計が変更されています
錯体はRuからIrに、ピレンは無置換から二置換型のdi tert-Py(dtPy)に、アミンはジイソプロピルエチルアミン(DIPEA)からジメチルアニリン(DMA)へと置き換わっています
このように反応系がデザインされたことで、従来との相違点を数多く生じることとなりました
この点については、次のように列挙できます
- DMAは基質との再結合能が低い[6]
- dtPyのtBu基は凝集を抑制し、励起状態の失活を起きにくくします。これによって、無置換PyよりもTTA能が向上する
- Ir錯体はRu錯体に比べて安定であり、DMAによるreductive quenchを受けない
- Ir錯体の共存下であっても、三重項励起状態のdtPyの寿命は、DMA濃度に影響されない。このため、三重項励起状態のdtPyは直接的にdtPyのラジカルアニオン状態とならない
- Ir錯体の安定性のため、dtPyのラジカルアニオンはIr錯体を還元できない。このためdtPyのラジカルアニオンは長い時間存在でき、過渡吸収分光法によって観測できる
このように多くの工夫がなされたことでsTTA-UCパスが顕在化し、初めてその有効性が示されました
③Consecutive photoinduced electron transfer (ConPET)
本シリーズの冒頭では、Photoredox触媒が光励起によって酸化や還元反応を起こしやすくなることについて解説しました
このような、光励起を伴う電子移動機構をPhotoinduced electron transfer (PET)機構と呼びます
このPET機構においては、酸化や還元によって新たに生成したphotoredox触媒の活性種は、さらに光励起されることで新たな活性種を生成する場合があります
この機構は、PET機構とは区別してconsecutive PET(conPET)機構と呼び、より高いエネルギーを必要とする反応に適用可能です
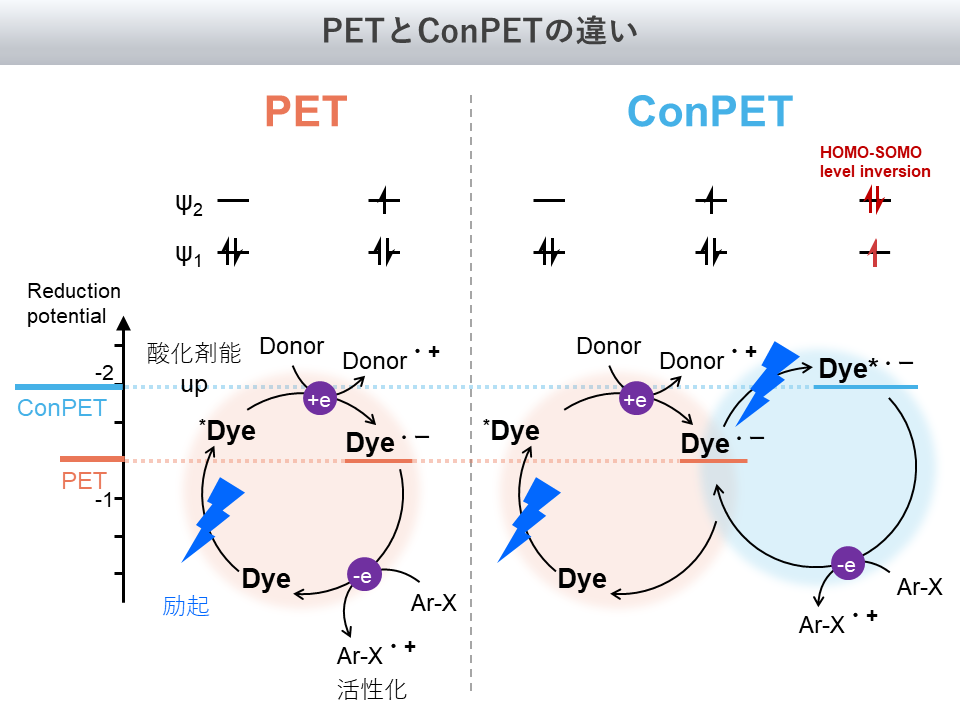
これを図式として表したものが図8になります
ConPETにおける活性種はHOMO-SOMO level inversionを経由し、より不安定な電子配置をとります
これにより、ConPETにおける活性種は、PETにおける活性種よりも高い反応性を獲得することができます
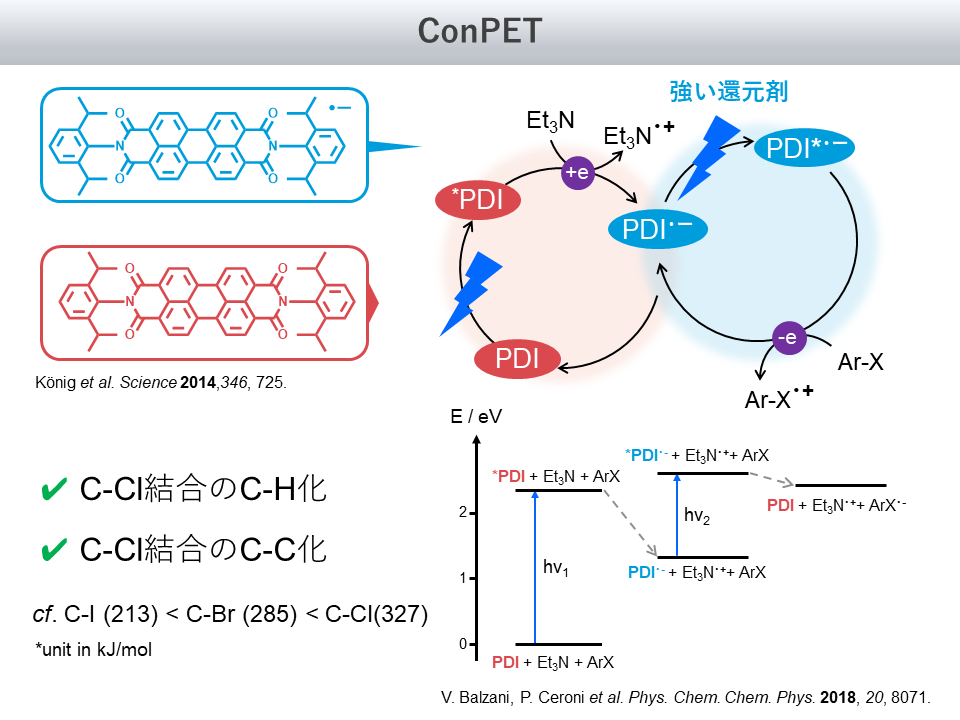
ConPETの一例を図9に示します
この例は2014年にKönig氏のグループから報告されたもので、ペリレンジイミド(PDI)を光触媒として用いています[8], [9]
スキームは左下にあるPDIの基底状態からスタートし、順に光吸収、アミンによる還元、2回目の光吸収、そして基質への還元と続きます
これによって、C-Cl結合といった強固な結合でさえも、C-H化やC-C化できることが見出されています
結論
以上では、低エネルギー光である可視光を用いた高エネルギー反応を3つ掲載しました
いずれも系中では電子移動やエネルギー移動を多段階に組み合わせ、適切にデザインされた反応経路をたどることによって、合成的価値の高い化学変換を達成しています
これらの反応は応用性に優れていることに加え、その複雑性ゆえに未知の部分も多く、当分は工学・理学の両側面からホットな分野であることが伺えます
本記事で紹介したものは有名な3パターンですが、他にも2光子吸収などといったエネルギー変換法も存在しており、利用する側の立場となると多くの選択肢が存在します
ぜひそれぞれの反応の得意・不得意を見極め、適切な利用法を見出すことによって、新たな価値の創出につなげましょう









コメントを残す
コメントを投稿するにはログインしてください。